Di dalam reaksi
kimia pereaksi berubah menjadi hasil reaksi. Laju dari perubahan zat
adalah ukuran jumlah perubahan zat yang terjadi tiap satuan waktu.
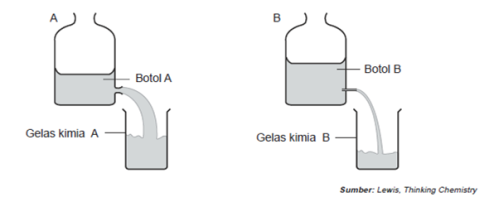 Pada
Gambar di atas, air dialirkan dari botol besar ke gelas kimia. Lubang
untuk aliran kedua botol tersebut berbeda. Pada botol yang mana laju
aliran air yang lebih cepat? Dari percobaan ini, laju dapat ditentukan
dengan dua cara yaitu dengan mengukur volum air yang berkurang dari
botol per satuan waktu dan volum air yang bertambah pada gelas kimia per
satuan waktu. Dari ilustrasi tersebut maka untuk mengukur laju reaksi
dapat ditentukan dengan dua cara yaitu dengan mengukur:
Pada
Gambar di atas, air dialirkan dari botol besar ke gelas kimia. Lubang
untuk aliran kedua botol tersebut berbeda. Pada botol yang mana laju
aliran air yang lebih cepat? Dari percobaan ini, laju dapat ditentukan
dengan dua cara yaitu dengan mengukur volum air yang berkurang dari
botol per satuan waktu dan volum air yang bertambah pada gelas kimia per
satuan waktu. Dari ilustrasi tersebut maka untuk mengukur laju reaksi
dapat ditentukan dengan dua cara yaitu dengan mengukur:
1. jumlah pereaksi yang digunakan atau bereaksi per satuan waktu, dan
2. jumlah hasil reaksi yang terbentuk per satuan waktu.
Misalnya pada saat mereaksikan logam
magnesium dengan asam klorida dengan reaksi: Mg(s) + 2 HCl(aq) ®
MgCl2(aq) + H2(g) Laju reaksi dapat dihitung dengan mengukur jumlah
magnesium atau asam klorida yang digunakan dalam waktu tertentu atau
jumlah magnesium klorida atau gas hidrogen yang terbentuk dalam waktu
tertentu.
Dalam beberapa reaksi, pereaksi dan hasil
reaksi dalam keadaan bercampur dan dalam wujud yang sama. Untuk
memisahkannya cukup sulit. Oleh karena itu, pengukuran laju reaksi akan
lebih mudah pada reaksi yang wujud hasil reaksinya berbeda dengan
pereaksi. Pengukuran laju reaksi yang menghasilkan gas dapat dilakukan
dengan mengukur volum gas yang terjadi dalam waktu yang ditentukan atau
mengukur massa setelah beberapa waktu yang ditentukan.
1. Menghitung Laju Reaksi dengan Mengukur Perubahan Volum
Sebagai contoh pengukuran laju reaksi untuk reaksi logam dengan asam. Perhatikan Gambar berikut:
Gambar : Mengukur laju reaksi dengan mengukur perubahan volum
 Pada
percobaan ini digunakan labu erlenmeyer berlengan. Pada saat logam
dimasukkan ke dalam larutan asam, labu erlenmeyer segera di tutup. Asam
dan logam akan bereaksi menghasilkan gas. Gas yang terbentuk akan
menekan air sehingga volum gas dapat diukur. Volum gas diukur tiap
menit. Hasil percobaannya dapat dilihat pada Tabel berikut.
Pada
percobaan ini digunakan labu erlenmeyer berlengan. Pada saat logam
dimasukkan ke dalam larutan asam, labu erlenmeyer segera di tutup. Asam
dan logam akan bereaksi menghasilkan gas. Gas yang terbentuk akan
menekan air sehingga volum gas dapat diukur. Volum gas diukur tiap
menit. Hasil percobaannya dapat dilihat pada Tabel berikut.
Tabel: Hasil pengukuran volum gas yang terbentuk dari reaksi asam dan logam
Data percobaan tersebut dapat dibuat grafik seperti Gambar berikut:
Gambar : Grafik antara volum gas yang dihasilkan dari reaksi asam danlogam dengan waktu (menit)
 Dari
data percobaan dapat dilihat reaksi mula-mula sangat cepat gas yang
dihasilkan 12 mL dalam waktu 1 menit. Tetapi setelah 5 menit hanya 3 mL
dan setelah 9 menit tidak ada lagi gas yang dihasilkan, artinya reaksi
telah selesai. Untuk menentukan laju reaksinya diambil dari kemiringan
(gradien) kurva pada waktu-waktu tertentu dan menggambarkan tangens pada
kurva. Langkahlangkahnya yaitu:
Dari
data percobaan dapat dilihat reaksi mula-mula sangat cepat gas yang
dihasilkan 12 mL dalam waktu 1 menit. Tetapi setelah 5 menit hanya 3 mL
dan setelah 9 menit tidak ada lagi gas yang dihasilkan, artinya reaksi
telah selesai. Untuk menentukan laju reaksinya diambil dari kemiringan
(gradien) kurva pada waktu-waktu tertentu dan menggambarkan tangens pada
kurva. Langkahlangkahnya yaitu:
a. Buat garis miring pada titik yang menunjukkan waktu 2 menit.
b. Gambarkan tangens pada kurva.
c. Ukur perubahan jarak vertikel dan perubahan jarak horisontal.
Hitung kemiringan (gradien) dengan rumus:
Perhatikan Gambar Berikut:
Gambar : Menentukan gradient
 Pada diagram, perubahan jarak vertikal = perubahan volum
Pada diagram, perubahan jarak vertikal = perubahan volumdan Perubahan jarak horisontal = perubahan waktu.
Gradien pada grafik
menunjukkan perubahan volum per satuan waktu atau laju reaksi, maka laju
reaksi di atas adalah 6 mL per menit. Artinya setiap 1 menit dihasilkan
6 mL hidrogen.
2. Menghitung Laju Reaksi melalui Perubahan Massa
Metode ini cocok untuk reaksi yang
menghasilkan gas dengan massa cukup tinggi seperti CO2. Misalnya reaksi
antara CaCO3 dengan HCl. Persamaan reaksi:
Berikut ini adalah cara
mengukur perubahan massa zat selama reaksi dan perhitungan laju
reaksinya berdasarkan grafik perubahan massa zat selama reaksi.
Perhatikan Gambar berikut:
Gambar : Mengukur laju reaksi melalui perubahan massa
Pada percobaan ini sistem yang terdiri
dari zat yang direaksikan dan peralatan diletakkan pada timbangan
digital. Kaca arloji penutup gelas kimia diganjal sehingga ada celah
kecil agar gas dapat keluar. Akibat gas hasil reaksi keluar maka massa
sistem setiap waktu akan berkurang. Hasil pengamatan pengukuran massa
setiap menit dibuat grafik misalnya seperti Gambar dibawah.
Gambar : Menentukan gradient
Jika pada percobaan yang diukur adalah perubahan konsentrasi seperti padagrafik berikut.
Gambar : Grafik konsentrasi terhadap waktu
Kemiringannya dapat dihitung dengan rumus:
Berdasarkan grafik di atas dapat disimpulkan bahwa
laju reaksi adalah perubahan konsentrasi pereaksi atau hasil reaksi per
satuan waktu. Laju reaksi dapat dirumuskan sebagai berikut.Untuk perubahan konsentrasi pereaksi
Tanda negatif menunjukkan konsentrasi pereaksi berkurang selama bereaksi
Untuk perubahan konsentrasi hasil reaksi :

r = laju reaksi
DC = perubahan konsentrasi
Dt = perubahan waktu
Satuan untuk laju reaksi adalah mol liter–1 detik–1 atau M detik–1.











Tidak ada komentar:
Posting Komentar